Biotecnología
La defensa antioxidante en las plantas: Una herramienta clave para la fitorremediación
The antioxidant defense in plants: A key tool for phytoremediation
M. del R. Peralta-Pérez1 y T.L. Volke-Sepúlveda2*
1 Facultad de Ciencias Químicas, Universidad Autónoma de Chihuahua. Circuito No. 1, Nuevo Campus Universitario; Chihuahua 31125, México. AP 669 y 1542-C.
2 Departamento de Biotecnología, Universidad Autónoma Metropolitana - Iztapalapa. San Rafael Atlixco 186, Col. Vicentina, México 09340 D.F.*Autora para la correspondencia. E-mail: tvs@xanum.uam.mx Fax (55) 58 04 64 07
Recibido 20 de Septiembre 2011
Aceptado 23 de Noviembre 2011
Aceptado 23 de Noviembre 2011
Resumen
La fitorremediación es una alternativa viable para tratar suelos contaminados con metales/metaloides y compuestos orgánicos. Durante la última década, numerosos estudios han demostrado su potencial para remediar suelos; no obstante, para superar algunas de sus limitaciones es importante continuar realizando investigación. De acuerdo con las características del contaminante y sitio a tratar, la fitorremediación ocurre a través de diferentes procesos. Para contaminantes orgánicos, destacan la fitodegradación y la rizorremediación, mientras que para metales/metaloides, la fitoextracción y la fitoestabilización se encuentran entre las escasas alternativas aplicables. En cualquier caso, para que la fitorremediación de un sitio sea posible, las plantas y microorganismos involucrados deben tolerar al contaminante en particular. Un mecanismo que determina el grado de tolerancia de un organismo a un contaminante, es la activación de una red de defensa antioxidante que elimina el exceso de especies reactivas de oxígeno (ERO) producidas en presencia del contaminante. Así, el desequilibrio en los niveles de ERO genera un incremento en el estrés oxidativo que, finalmente, conduce a severos daños celulares. El objetivo de este documento es revisar el potencial de los diferentes procesos de fitorremediación para tratar suelos contaminados, así como la importancia del control del estrés oxidativo como una estrategia de las plantas para tolerar la presencia de contaminantes.
Palabras clave: fitorremediación, suelos, metales, xenobióticos, estrés oxidativo.
Abstract
Phytoremediation is a feasible alternative to treat soils polluted with metals/metalloids and organic compounds. During the last decade, several studies have demonstrated its potential for soil remediation; however, to overcome some of its limitations is important to continue conducting research. According to the characteristics of the pollutant and the site to be treated, phytoremediation occurs through different processes. For organic contaminants, rhizoremediation and phytodegradation have been the leading options, while for metals/metalloids phytoextraction and phytostabilization are among the few applicable alternatives. In any case, in order to phytoremediate a site, the involved plants and microorganisms must be tolerant to the particular pollutant. A mechanism that determines the tolerance degree of an organism to a pollutant is the activation of an antioxidant defense network that removes the excess of reactive oxygen species (ROS) produced in presence of the pollutant. Thus, the imbalance in the ROS levels produces an increase in the oxidative stress that eventually leads to severe cell damage. The aim of this paper ts to review the potential of the different phytoremediation processes to treat polluted soils, as well as the importance of controlling the oxidative stress as a plant strategy to tolerate the presence of pollutants.
Keywords: phytoremediation, soils, metals, xenobiotics, oxidative stress.
1 Introducción
La creciente industrialización en la economía global durante el último siglo ha conducido a un dramático aumento en la liberación al ambiente de diversos contaminantes orgánicos e inorgánicos, tales como sales, metales pesados, solventes, hidrocarburos y pesticidas, entre otros. La mayoría de estos contaminantes no se degrada fácilmente, conduciendo a su acumulación en los suelos (Gerhardt y col. 2009). Los métodos fisicoqúmicos tradicionales (incineración, solidificación/estabilización, lavado, excavación y entierro) para la limpieza de suelos contaminados son caros - 25 a 50 mil millones de USD por año, a nivel mundial (Pilon-Smits, 2005) - y, generalmente, se consideran como una primera acción para sitios muy contaminados. Por lo tanto, no son muy adecuados para remediar grandes áreas, donde los contaminantes se encuentran dispersos en concentraciones bajas a moderadas. En tal caso, la fitorremediación es una alternativa económicamente factible (Garbisu y Alkorta, 2001; Singh y col., 2003).
La fitorremediación implica la acción de varios procesos que utilizan plantas y los microorganismos asociados a su rizosfera para remediar ambientes contaminados - principalmente suelo y agua -mediante la remoción, transformación, degradación o estabilización de contaminantes orgánicos e inorgánicos (Meagher, 2000; Mench y col., 2009). Aunque el uso de plantas para remediar suelos contaminados con elementos radiactivos se exploró desde los años 50, el termino fitorremediación se adopto hasta los años 80, y fue en la última década cuando su uso comenzó a expandirse rápidamente (Gerhardt y col., 2009). A la fecha, esta tecnología se ha explorado, implementado y/o demostrado como una alternativa efectiva y económicamente rentable para la limpieza in situ de diversos tipos de contaminantes, cuya expansión y aplicación ha sido posible gracias a la creciente investigación en el campo. Durante la última década, se publicó un total de 3537 documentos científicos (artículos, memorias en extenso y revisiones) en diversos campos de la fitorremediación (Fig. 1), destacando los relacionados con metales (1527 publicaciones, con 18 citas promedio por publicación) e hidrocarburos (369, 15 citas promedio), entre otros contaminantes como pesticidas (121, 15 citas promedio), herbicidas (69, 16 citas promedio), explosivos (65, 19 citas promedio) y bifenilos policlorados (60, 15 citas promedio) (ISI Web of Knowledge, 2011).
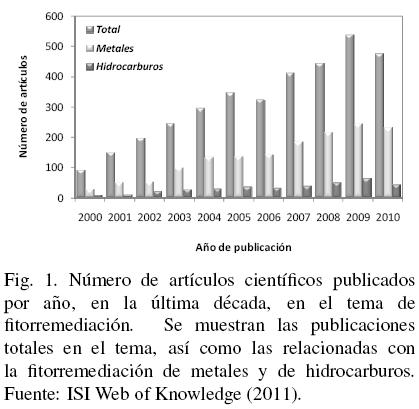
Los contaminantes pueden clasificarse como orgánicos (susceptibles de biodegradación) e inorgánicos (no biodegradables). La mayor parte de los contaminantes orgánicos (CO) son moléculas xenobióticas y tóxicas para los organismos, y son liberados al ambiente principalmente a través de derrames y por actividades agrícolas e industriales. Dependiendo de sus propiedades, pueden degradarse en la rizósfera o ser absorbidos, degradados, secuestrados y/o volatilizados por plantas. Este tipo de contaminantes incluye residuos domésticos e industriales, derivados del petróleo, aguas residuales, pesticidas e insecticidas, entre otros. En contraste, los contaminantes inorgánicos (CI) no se biodegradan, pero pueden ser estabilizados o acumulados por la acción de ciertas plantas (Pilon-Smits, 2005). Muchos CI se encuentran naturalmente en la corteza terrestre o la atmósfera, pero actividades humanas como la minería, industria, agricultura y actividades militares promueven su liberación al ambiente. Estos incluyen compuestos como nitratos y fosfatos, cianuros, metales y metaloides y algunos isotopos radioactivos. En Europa, los contaminantes mas frecuentes en suelos son aceite mineral (38%), metales y metaloides (37%) e hidrocarburos aromáticos policíclicos (HAP, 13%)(Mench y col., 2009).
Además de la amplia gama de contaminantes que puede tratarse, de su aceptación pública y de los bajos costos para su implementación, la fitorremediación ofrece varias ventajas (Pilon-Smits, 2005; Mench y col., 2009): (i) depende de energía solar y su mantenimiento es mínimo; (ii) puede aplicarse in situ en grandes áreas; (iii) es una opción potencialmente permanente que reduce la erosión; (iv) evita la destrucción de la estructura del suelo y la contaminación secundaria; (v) la generación de residuos y emisiones es mínima. Hoy en día, varios procesos de fitorremediación se encuentran a nivel demostrativo y algunas ya se aplican en grandes sitios (Mench y col., 2009). No obstante, entre las principales limitaciones para su aplicación se encuentran la lentitud del proceso, la toxicidad de altas concentraciones de contaminantes para plantas y microorganismos, y el riesgo de la posible entrada de contaminantes en la cadena trófica (Singh y col., 2003; Pilon-Smits, 2005; Mench y col., 2009). Algunas de estas limitaciones pueden superarse, al menos en parte, a través de un mayor entendimiento acerca de la forma en que las plantas y microorganismos asociados pueden acumular, excluir y metabolizar CO y CI.
Aunado a lo anterior, cada sitio contaminado es diferente y la forma de manejarlo requiere una cuidadosa ponderación de todos los factores relevantes dentro de los límites establecidos por la legislación, la aceptación social y el financiamiento disponible (Mench y col., 2009). Con base en lo anterior, en este trabajo se revisan los procesos de fitorremediación aplicables a suelos contaminados con CO y CI, así como la importancia del control del estrés oxidativo como una estrategia de las plantas para tolerar y detoxificar dichos contaminantes.
2 Procesos de fitorremediación
En general, la meta de cualquier tecnología de remediación, in situ o ex situ, implica la remoción de los contaminantes (descontaminación o limpieza), o bien, la reducción del riesgo asociado a su presencia limitando la exposición (estabilización) (Vangronsveld y col. 2009). Así, la fitorremediación de un suelo puede lograrse a través de la acción de uno o varios de los siguientes procesos: fitodegradación, fitoextracción, fitovolatilización, fitoestabilización y/o rizorremediación (Fig. 2). El proceso a través del cual una planta actúa sobre un contaminante en particular, depende del grado de contaminación, de las características fisicoquímicas del contaminante y del sitio contaminado, así como de las propiedades fenotípicas y genotípicas de cada especie vegetal, tales como su grado de tolerancia y su capacidad para captar, absorber, acumular y/o degradar los contaminantes (Meagher 2000; Vangronsveld y col. 2009). De tal manera que un proceso efectivo para la remoció n de un contaminante en particular puede ser inutil para otro. Por ejemplo, la fitoextracción y la fitoestabilización pueden ser procesos muy efectivos para la remoción de sales y metales pesados de un suelo, pero poco útiles en la limpieza de ciertos hidrocarburos y explosivos, para los que la fitodegradación o la rizorremediación serían mucho más efectivos.
Como puede verse, diversos contaminantes pueden ser metabolizados, estabilizados en el suelo o extraídos del mismo a través de uno u otro proceso de fitorremediación, con la ventaja adicional de que el uso de plantas permite el control de la erosión y la evapotranspiración de grandes cantidades de agua. En el caso de CO, la fitorremediación implica su captación y translocación a los tejidos aéreos, para su metabolismo o volatilización y, en ocasiones, su mineralización hasta moléculas como CO2, NO3 y NH4 (Eapen y col., 2007). CO de bajo peso molecular pueden ser removidos del suelo y liberados a la atmosfera a través de las hojas por evapotranspiración(fitovolatilización). CO no volatiles pueden ser degradados o convertidos a formas menos tóxicas por vía enzimatica (fitodegradación) o secuestrados por la planta (fitoextracción) (Gerhardt y col., 2009). Otro proceso común para CO, es la degradación por microorganismos de la rizosfera (rizorremediación), cuyo crecimiento es estimulado por componentes de los exudados radiculares (Meagher, 2000; Eapen ycol., 2007).
Para CI como metales y metaloides, la fitorremediación implica: (i) la absorción del elemento por la planta, seguida por su translocación y acumulación en tejidos aéreos (fitoextracción) o, en el caso de elementos volátiles (As, Se y Hg), su transformación a formas menos tóxicas y su liberación a la atmosfera (fitovolatilización); (ii) la transformación a especies químicas menos tóxicas y/o solubles por acción de exudados radiculares (fitoestabilización); (iii) la inmovilización del elemento por su acumulación en las raíces o su incorporación a lignina o humus (fitoestabilización) (Meagher, 2000; Kavamura y Esposito, 2010). Todos estos procesos pueden mejorarse a través de la asociación entre plantas y microorganismos rizosféricos (rizorremediación) (Kuiper y col., 2004; Kidd y col., 2009).
Entre los CO que han sido tratados por fitorremediación (Tabla 1), se encuentran moléculas halogenadas como tricloroetileno (TCE), 2,4-diclorofenol y bifenilos policlorados (PCB); pesticidas como clorpirifós, 1,1,1-tricloro-2,2,-bis-(4'-clorofenil)-etano (DDT) y dibromuro de etileno (EDB); explosivos como trinitrotolueno (TNT), dinitrotolueno (DNT), nitroglicerina y hexahidro-l,3,5-trinitro-l,3,5-triazina (RDX); hidrocarburos aromáticos policíclicos (PAH), hidrocarburos del petróleo (TPH) y detergentes (Eapen y col, 2007; Gerhardt y col, 2009). Por su parte, los CI susceptibles de fitorremediarse incluyen metales como Pb, Zn, Cd, Cr, Co, Cu, Ni y Hg, metaloides como As y Se, elementos radioactivos (90Sr, 137Cs, 238U) y compuestos que contienen sodio, nitratos, amonio y fosfatos (Pilon-Smits, 2005).
A la fecha, los procesos de fitorremediación con mayor atención científica y comercial han sido la rizorremediación y la fitoextracción (Tabla 1). Esta última es una de las pocas opciones para tratar sitios contaminados con metales y metaloides mediante el uso de plantas hiperacumuladoras1 como Brassica juncea (hiperacumuladora de Pb, Ni y Cd), Thlaspi caerulescens (Zn), Helianthus annuus (Cr(III)) (de la Rosa y col., 2008) y Prosopis laevigata (Pb y Ni) (Buendía-González y col., 2010). Este proceso puede mejorarse por adición de agentes quelantes, no obstante, éstos también aumentan la lixiviación de metales en el suelo y pueden afectar el crecimiento vegetal, por lo que su uso debe ser estrictamente controlado (Chen y col, 2004). Por su parte, la rizorremediación ha mostrado ser particularmente efectiva para la remoción y/o degradación de CO, especialmente cuando se usa junto con técnicas agronómicas adecuadas (Wenzel y col, 2003; Gerhardt y col, 2009). Una estrategia para inducir y favorecer la rizorremediación es la bioaumentación con microorganismos que degradan los contaminantes de interés. Los grupos microbianos mas estudiados en este campo son las rizobacterias promotoras del crecimiento vegetal y los hongos micorrícicos.
Otro proceso de gran importancia, en particular para la recuperacion de zonas mineras, debido a las grandes extensiones afectadas, es la fitoestabilización (Tabla 1). Análogo al uso de plantas hiper-acumuladoras para la fitoextracción, las plantas adecuadas para fines de fitoestabilización se conocen como exclusoras2. Para tal propósito, se ha demostrado el potencial de pastos y árboles que, además de tolerar condiciones de estrés, tienen altas tasas de producción de biomasa, sistemas radiculares extensos y, en muchas ocasiones, una baja translocación del contaminante a la parte aérea (Euliss y col., 2008). Uno de los géneros de pastos más estudiados para tal propósito es Vetiveria (Chiu y col., 2006) y también se ha demostrado la capacidad de algunas especies de Festuca (Frérot y col., 2006). Entre los árboles, se ha demostrado que géneros como Fraxinus, Alnus, Acer y Robinia pueden ser adecuados para fitoestabilizar residuos con metales (Mertens y col., 2004).
3 La defensa antioxidante y la tolerancia a contaminantes
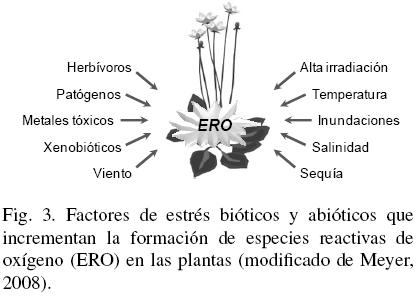
Independientemente del proceso de fitorremediación, para que este ocurra de forma eficiente, las plantas y microorganismos involucrados deben ser tolerantes al contaminante en particular. Uno de los mecanismos a través del cual los organismos toleran la presencia de contaminantes, es la activación de sistemas de defensa que suprimen o eliminan especies reactivas de oxígeno (ERO). La producción celular de ERO es estimulada en respuesta a desbalances metabólicos generados por una condición de estrés que rompe la homeostasis3 celular (Mittler, 2002; Meyer, 2008). Una serie de factores bióticos y abióticos (Fig. 3), entre ellos la presencia de contaminantes, modifica el equilibrio entre la producción y la eliminación de ERO e induce un fenómeno conocido como estrés oxidativo (Rinalducci y col., 2008; Gill y Tuteja, 2010).
3.1 Producción de especies reactivas de oxígeno y sus efectos en las células
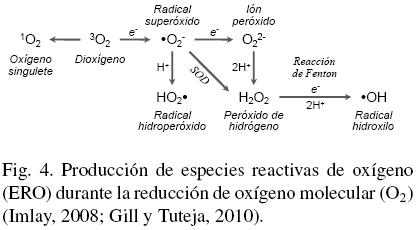
El estrés oxidativo se define como el efecto tóxico provocado por especies químicas altamente reactivas producidas durante la reducción del oxígeno molecular (O2) en los organismos aerobios, que pueden ser o no radicales libres4 (Halliwell, 2006) y se conocen como ERO (Rinalducci y col., 2008). La reducción del O2 ocurre en varios pasos (Fig. 4): (i) la primera reducción produce radicales superóxido (·O-2) o hidroperoxido (HO2); (ii) de forma enzimatica (por la superoxido dismutasa, SOD) o espontanea (mediante la perdida de otro electrón), el ·O-2 es dismutado a peróxido de hidrógeno (H2O2) (Gechev y col., 2006); (iii) el H2O2 puede ser transformado al radical hidroxilo (·OH) por la reacción Fenton, o bien, eliminado por acción de catalasas o del ciclo ascorbato-glutatión (Blokhina y col., 2003; Rinalducci y col., 2008). El oxígeno singulete (1O2) es otra ERO que no se relaciona con la transferencia de electrones (e-), ya que es el primer estado excitado del O2, producido por foto-activación (Triantaphylides y Havaux, 2009). En las plantas, las ERO se producen en varios compartimentos celulares, principalmente en cloroplastos y mitocondrias, a través de la fuga de e~ de las cadenas transportadoras al O2. Los cloroplastos son los principales productores de lOi en el fotosistema II y de ·O-2 en el fotosistema I. La respiración mitocondrial también produce cantidades importantes de ·O-2. En el apoplasto, la actividad de oxidasas y peroxidasas es la principal fuente de ·O-2, mientras que en los peroxisomas la fotorespiración genera H2O2 (Gechev y col., 2006; Halliwell, 2006).
Aunque todas las ERO son muy reactivas, cada una tiene propiedades diferentes y reacciona con diferentes moléculas. El ·O-2 tiene un tiempo de vida media (τ1/2) de 2-4 yus y aunque difícilmente reacciona con lípidos, puede inactivar enzimas con centros Fe-S. El H2O2 (τ1/2 ~ 1 ms) es relativamente estable y su concentración normal en las plantas se encuentra en el rango μM - mM (~0.5 μM en cloroplastos). Esta ERO no reacciona fácilmente con lípidos, carbohidratos o ADN, pero puede inactivar enzimas mediante la oxidación de grupos tiolicos. El HO2. puede atravesar membranas y oxidar lípidos por la sustracción de protones de ácidos grasos poli-insaturados (PUFA). El 1O2 (τ1/2 ~ 1 μs) es particularmente reactivo con dobles enlaces conjugados como los de PUFA y aminoacidos aromáticos (Mittler, 2002; M0ller y col., 2007; Rinalducci y col., 2008). Las propiedades tóxicas del ·O-2 y el H2O2 aumentan en presencia de metales redox-activos (Fe3+ y Cu2+), ya que forman el radical OH a través la reacción Haber-Weiss5 (Fig. 4). El OH (t1/2 ~ 1 ns) es la ERO mas reactiva, reacciona rápidamente con todo tipo de macromoléculas y no hay un mecanismo enzimático que la elimine, por lo que su sobreproducción finalmente conduce a la muerte celular (Gechev y col., 2006; Møller y col., 2007; Sharma y Dietz, 2008; Gill y Tuteja, 2010).
En cualquier caso, si la concentración intracelular de ERO no es controlada, la consecuencia directa es el daño a estructuras celulares debido a la peroxidación de lípidos, oxidación de proteínas y componentes del ADN, así como la interrupción de rutas metabolicas como la asimilativa del azufre (Blokhina y col., 2003; Møller y col., 2007; Imlay, 2008).
3.2 Mecanismos de defensa antioxidante
Es claro que el incremento la acumulación de ERO representa una amenaza, por lo que un estricto control en sus niveles es esencial para evitar su toxicidad celular y asegurar sus funciones de señalización, como son el control de la proliferación y muerte celular, la adaptación a factores de estrés abiótico y las respuestas al ataque de patógenos (Liu y col., 2009; Gill y Tuteja, 2010). Los niveles celulares de ERO son estrictamente regulados por una compleja red de defensa antioxidante, que incluye reacciones enzimáticas y moléculas amortiguadoras antioxidantes que, junto con las enzimas productoras de ERO, mantienen la homeostasis en todos los compartimentos celulares (Gechev y col., 2006; Martí y col., 2009). Así, la red de defensa antioxidante actúa controlando las cascadas de oxidación y protegiendo a las células contra daños oxidativos. Esta defensa puede actuar (i) minimizando la producción de ERO; o (ii) eliminando las ERO producidas, reduciendo la posibilidad de un eventual daño celular (M0ller, 2001; Gratão y col., 2005).
I. Minimización de la producción de ERO. La primera línea de defensa contra el estrés oxidativo en plantas actúa reduciendo la producción de ERO mediante procesos como: (i) adaptaciones anatómicas y fisiológicas; (ii) mecanismos que reorganizan el aparato fotosintético o suprimen la fotosíntesis; (iii) acción de un grupo de enzimas llamadas oxidasas alternativas (AOX) que pueden desviar e- que fluyen a través de las cadenas transportadoras durante la respiración y usarlos para reducir O2 a H2O, evitando la formación de ·OH (Møller, 2001; Mittler, 2002); (iv) prevención de la formación de ·OH mediante la eliminación de ·O2- y H2O2 y/o el secuestro de iones que catalizan la reacción Haber-Weiss, por su unión a proteínas como ferritinas o metalotioneinas (Gechev y col., 2006).II. Eliminación de ERO. La eliminación de ERO actúa como una segunda línea de defensa, a través de la acción de moléculas antioxidantes6 y de varias enzimas que interactúan directamente con ERO y regeneran las formas reducidas de las moléculas antioxidantes mediante el ciclo ascorbato-glutatión (Blokhina y col., 2003).
Moléculas antioxidantes. En las células vegetales, los antioxidantes más importantes que regulan la homeostasis de ERO son el ascorbato (ASC) y el glutatión (GSH), además de taninos, flavonoides, α-tocoferol, carotenoides y precursores de la lignina (Apel y Hirt, 2004). Estas moléculas actúan como una red que, a través de una serie de reacciones redox, evita el daño por ERO (Blokhina y col., 2003; Gratão y col., 2005). Los carotenoides y flavonoides neutralizan ERO como H2O2, ·OH y 1O2. El α-tocoferol es el principal antioxidante liposoluble en las membranas fotosinteticas, donde elimina 1O2 y protege los lípidos contra peroxidación (Gechev y col., 2006). El ASC es el más abundante y poderoso antioxidante hidrosoluble que protege las membranas mediante la reducción de la forma oxidada del a-tocoferol y por la eliminación directa de ·O2- y ·OH; es además sustrato de la APX, que cataliza la reducción de H2O2 (Fig. 5). El GSH se considera la defensa más importante contra ERO, además de estar involucrado en funciones vitales como el transporte y almacenamiento de azufre reducido, la protección contra metales tóxicos como precursor de fitoquelatinas y la detoxificación de xenobióticos a través de reacciones de conjugación por la glutatión-S-transferasa (Mittler, 2002; Martí y col., 2009; Gill y Tuteja, 2010).
Enzimas que interactúan con ERO. Como se mencionó , las plantas poseen un complejo sistema enzimático antioxidante en diferentes compartimentos celulares. Se ha reportado que entre 1 y 2% del O2 consumido por estos organismos conduce a la formación del radical -O- (Gill y Tuteja, 2010). La superoxido dismutasa (SOD) es la unica enzima en las plantas que dismuta el ·O2- en H2O2 y O2. El H2O2 puede ser directamente catabolizado por catalasas (CAT) o, en presencia de sustratos reductores, por varios tipos de peroxidasas, en el ciclo ascorbatoglutatión (Fig. 5) (Gechev y col., 2006; Halliwell, 2006; Martí y col., 2009).
Ciclo ascorbato-glutatión. Este ciclo juega un papel central en la integración de la señalización redox y se considera la principal ruta de eliminación del H2O2 producido a partir del ·O2-, a través de una serie de reacciones redox que incluye la oxidación de GSH y ASC por H2O2 (Fig. 5a) (Apel y Hirt, 2004; Tausz y col., 2004; Meyer, 2008). La conversión de H2O2 a H2O por la ascorbato peroxidasa (APX) ocurre por la oxidación del ASC a monodehidro-ascorbato (MDA), que puede regenerarse por la monodehidro-ascorbato reductasa (MDAR) con NAD(P)H como reductor. El MDA puede dismutarse espontáneamente en dehidro-ascorbato (DHA) por la oxidación de GSH a GSSG. Finalmente, la glutatión reductasa (GR) puede regenerar GSH a partir de glutatión disulfuro (GSSG), usando NAD(P)H como agente reductor (Fig. 5b). La glutatión reductasa (GR) también detoxifica H2O2 a H2(D, usando directamente GSH como reductor (Fig. 5c). Así, las formas oxidadas del ASC y el GSH son conducidas a sus estados reducidos iniciales, cerrando el ciclo y previniendo así la acumulación de H2O2 (Apel y Hirt, 2004; Liu y col., 2009; Martí y col, 2009).
3.3 Relación entre la tolerancia a contaminantes y la defensa antioxidante
Como se ha visto, la exposición de una planta a condiciones desfavorables puede inducir una condición de estrés que, a su vez, aumenta la producción de ERO incrementando el estrés oxidativo celular. En general, los estudios en el tema muestran que el impacto bioquímico de cada contaminante sobre las células vegetales es tan diverso como su naturaleza química, pero existe una clara relación entre el grado de tolerancia y la eficiencia de la red de defensa antioxidante.
La relación entre el desequilibrio en el estado celular redox y la fitotoxicidad por metales/metaloides se ha estudiado ampliamente y existen varias revisiones recientes del tema (Gratão y col., 2005; Sharma y Dietz, 2008; Franco y col., 2009; Mench y col., 2009). El principal mecanismo de toxicidad de estos contaminantes se relaciona con una sobreproducción de ERO, la cual modifica las defensas antioxidantes y provoca daños oxidativos en macromoléculas y cambios en la homeostasis del calcio y sulfhidrilos (Franco y col., 2009). Al respecto, la tolerancia en plantas tiene una fuerte correlación con altos niveles de GSH (Sharma y Dietz, 2008). Por ejemplo, Sun y col. (2005) y Singh y col. (2006) relacionaron la sobreproducción de GSH con la tolerancia a Pb y As por Sedum alfredii y Pteris vittata, respectivamente. Otro trabajo con plantas de Acacia farnesiana expuestas a Pb, también evidenció un papel clave del GSH en la detoxificación de ERO a través de la GR (Maldonado y col., 2011).
Por otra parte, los CO tienden a ser menos fitotoxicos debido, en parte, a que no se acumulan tan fácilmente y a que suelen ser menos reactivos (Pilon-Smits, 2005). Aunque la información acerca del impacto de CO sobre las plantas es más escasa, muchos de sus efectos tóxicos se relacionan con el estrés oxidativo (Franco y col., 2009), así como la tolerancia con la actividad antioxidante. Al respecto, Alkio y col. (2005) y Liu y col. (2009) demostraron que la exposición de Arabidopsis thaliana a HAP estimulo la producción de ERO. Marti y col. (2009) relacionaron el aumento en la actividad de enzimas antioxidantes con la tolerancia de plantas de Medicago sativa a lodos de petróleo. En Nicotiana tabacum y Melilotus albus crecidas con fenol (Ibáñez y col., 2011) y diesel (Hernández-Ortega y col., 2011) respectivamente, también se registro una sobreproducción de ERO que estimuló la actividad de enzimas antioxidantes. Asimismo, el aumento en los niveles de GSH y de las enzimas que lo sintetizan contribuye a la protección contra las ERO. Karavangeli y col. (2005) encontraron que la mayor tolerancia a alaclor en alamos se correlaciono con un aumento en la expresión de la y-glutamil-cisténa sintetasa. Esta misma enzima, junto con la GSH sintetasa, sobreexpresadas en B. juncea estimularon la tolerancia a atrazina, 1-cloro-2,4-dinitrobenceno (CDNB), matolaclor y fenantreno (Flocco y col., 2004).
Conclusiones y perspectivas
En 2010 se publicaron casi 480 artículos en el tema de la fitorremediación, contrastando con solo 93 en 2000. Este aumento en la investigación durante la última década, ha permitido un mayor conocimiento acerca de diversos aspectos en el tema, demostrando así la viabilidad de la tecnología para tratar suelos contaminados con niveles moderados de contaminantes orgánicos e inorgánicos, que puede aplicarse junto con o en lugar de costosos métodos fisicoqúmicos. Esta tecnica depende de energía solar, por lo que su mantenimiento y la generación de residuos y emisiones son mínimos, además de que es una opción potencialmente permanente que reduce la erosión y destrucción del suelo. El proceso más estudiado y con resultados más promisorios para tratar sitios con CO ha sido la rizorremediación, mientras que para el caso de metales y metaloides, la fitoextracción y la fitoestabilización se encuentran dentro de los escasos métodos aplicables y, por lo tanto, más estudiados. Los contaminantes más estudiados han sido herbicidas y HAP, además de elementos como Cd, Zn, Ni y As.
Una meta importante en el campo, es una mayor comprensión - a nivel fisiologico, bioqúmico y molecular - acerca de mecanismos de absorción-exclusión, translocación, acumulación, detoxificación y tolerancia al estrés en plantas y los microorganismos asociados, expuestos a un contaminante. Aunque estos procesos y su regulación aún no son del todo entendidos, la relación entre el grado de tolerancia a un contaminante y la eficiencia de la red de defensa antioxidante está demostrada. Esta red controla la sobreproducción de ERO inducida por la presencia de contaminantes, asegurando así sus funciones de señalización y evitando el estrés oxidativo. Las observaciones al respecto, indican que los organismos capaces de controlar eficientemente el nivel celular de ERO tienen potencial para su aplicación en fitorremediación, ya que pueden tolerar condiciones ambientales adversas. Así, la integración de estos conocimientos puede permitir optimizar estas propiedades en las plantas y microorganismos y conducir a superar las limitantes para su aplicación, abatiendo costos y mejorando los procesos implicados.
Referencias
Alkio, M., Tabuchi, T.M., Wang X. y Colón-Carmona A. (2005). Stress response to polycyclic aromatic hydrocarbons in Arabidopsis includes growth inhibition and hypersensitive responselike symptoms. Journal of Experimental Botany 56, 2983-2994. [ Links ]
Apel, K. y Hirt, H. (2004). Reactive oxygen species: metabolism, oxidative stress, and signal transduction. Annual Review of Plant Biology 55, 373-99. [ Links ]
Archer, M.J.G. y Caldwell, R.A. (2004). Response of six Australian plant species to heavy metal contamination at an abandoned mine site. Water, Air, and Soil Pollution 157, 257-267. [ Links ]
Blokhina, O., Virolainen, E. y Fagerstedt, K.V. (2003). Antioxidants, oxidative damage and oxygen deprivation stress: a review. Annals of Botany 91, 179-194. [ Links ]
Buendía-González, L., Orozco-Villafuerte, O., Estrada-Zuñiga, M.E., Barrera-Díaz, C.E., Vernon-Carter, E.J., Sosa-Cruz, F. (2010). Acumulación in vitro de plomo y níquel en plántulas de mezquite (Prosopis laevigata). Revista Mexicana de Ingeniería Química 9, 1-9. [ Links ]
Braud, A., Jezequel, K., Bazot, S. y Lebeau, T. (2009). Enhanced phytoextraction of an agricultural Cr- and Pb-contaminated soil by bioaugmentation with siderophore-producing bacteria. Chemosphere 74, 280-286. [ Links ]
Chen, Y., Li, X. y Shen, Z. (2004). Leaching and uptake of heavy metals by ten different species of plants during an EDTA-assisted phytoextraction process. Chemosphere 57, 187-196. [ Links ]
Chiu, K.K., Ye, Z.H. y Wong, M.H. (2006). Growth of Vetiveria zizanioides and Phragmities australis on Pb/Zn and Cu mine tailings amended with manure compost and sewage sludge: A greenhouse study. Bioresource Technology 97, 158-170. [ Links ]
de la Rosa, G., Cruz-Jiménez, G., Cano-Rodríguez, I., Fuentes-Ramírez, R., Gardea-Torresdey, J.L. (2008). Efecto de la edad de la planta y presencia de SS-EDDS en la tolerancia y absorción de Cr(III) por Helianthus annuus. Revista Mexicana de Ingeniería Química 7, 243-251. [ Links ]
Eapen, S., Singh, S. y D'Souza, S.F. (2007). Advances in development of transgenic plants for remediation of xenobiotic pollutants. Biotechnology Advances 25,442-451. [ Links ]
Euliss, K, Ho, C., Schwab, A.P., Rock, S. y Banks, M.K. (2008). Greenhouse and field assessment of phytoremediation for petroleum contaminants in a riparian zone. Bioresource Technology 99, 1961-1971. [ Links ]
Ferrera-Cerrato, R., Alarcón, A., Mendoza, M., Sangabriel, W., Trejo-Aguilar, D., Cruz-Sánchez, J.S., López-Ortiz, C. y Delgadillo-Martínez, J. (2007). Fitorremediación de un suelo contaminado con combustóleo utilizando Phaseolus coccineus y fertilización orgánica e inorgánica. Agrociencia 41, 817-826. [ Links ]
Fischerová, Z., Tlustos, P., Száková, J. y Sichorová, K. (2006). A comparison of phytoremediation capability of selected plant species for given trace elements. Environmental Pollution 144, 93-100. [ Links ]
Flocco, C.G., Lindblom, S.D. y Smits, E.A. (2004). Overexpression of enzymes involved in glutathione synthesis enhances tolerance to organic pollutants in Brassica juncea. International Journal of Phytoremediation 6, 289-304. [ Links ]
Franco, R., Sánchez-Olea, R., Reyes-Reyes, E.M. y Panayiotidis, M.I. (2009). Environmental toxicity, oxidative stress and apoptosis: Ménage a Trois. Mutation Research 674, 3-22. [ Links ]
Frérot, H., Lefebvre, C., Gruber, W., Collin, C., Dos Santos, A. y Escarre, J. (2006). Specific interactions between local metallicolous plants improve the phytostabilization of mine soils. Plant and Soil 282, 53-65. [ Links ]
Garbisu, C. y Alkorta, I. (2001). Phytoextraction: a cost-effective plant-based technology for the removal of metals from the environment. Bioresource Technology 77, 229-236. [ Links ]
Gechev, T.S., van Breusegem, F., Stone, J.M., Denev, I. y Laloi, C. (2006). Reactive oxygen species as signals that modulate plant stress responses and programmed cell death. BioEssays 28, 1091-1101. [ Links ]
Gerhardt, K.E., Huang, X.D., Glick, B.R. y Greenberg, B.M. (2009). Phytoremediation and rhizoremediation of organic soil contaminants: potential and challenges. Plant Science 176,20-30. [ Links ]
Gill, S.S. y Tuteja, N. (2010). Reactive oxygen species and antioxidant machinery in abiotic stress tolerance in crop plants. Plant Physiology and Biochemistry 48, 909-930. [ Links ]
Gratão, P., Polle, A., Lea, P.J. y Azevedo, R.A. (2005). Making the life of heavy metal-stressed plants a little easier. Functional Plant Biology 32, 481-494. [ Links ]
Halliwell, B. (2006). Reactive species and antioxidants. Redox biology is a fundamental theme of aerobic life. Plant Physiology 141, 312-322. [ Links ]
Hernández-Ortega, H.A., Alarcon, A., Ferrera-Cerrato, R., Zavaleta-Mancera, H.A., Lopez-Delgado, H.A. y Mendoza-Lopez, M.R. (2011). Arbuscular mycorrhizal fungi on growth, nutrient status, and total antioxidant activity of Melilotus albus during phytoremediation of a diesel-contaminated substrate. Journal of Environmental Management doi:10.1016/j.jenvman.2011.02.015 [ Links ]
Hsiao, K.H., Kao, P.H. y Hseu, Z.Y. (2007). Effects of chelators on chromium and nickel uptake by Brassica juncea on serpentine-mine tailings for phytoextraction. Journal of HazardousMaterials 148, 366-376. [ Links ]
Huang, X.D., El-Alawi, Y., Gurska, J., Glick, B.R. y Greenberg, B.M. (2005). A multi-process phytoremediation system for decontamination of persistent total petroleum hydrocarbons (TPHs) from soils. Microchemical Journal 81, 139-147. [ Links ]
Ibáñez, S.G., Medina, M.I. y Agostini, E. (2011). Phenol tolerance, changes of antioxidative enzymes and cellular damage in transgenic tobacco hairy roots colonized by arbuscular mycorrhizal fungi. Chemosphere 83, 700-705. [ Links ]
Imlay, J.A. (2008). Cellular defenses against superoxide and hydrogen peroxide. Annual Review of Biochemistry 77, 755-776. [ Links ]
Jiang, M., Cao, L. y Zhang, R. (2008). Effects of Acacia (Acacia auriculaeformis A. Cunn)-associated fungi on mustard (Brassica juncea (L.) Coss. var. foliosa Bailey) growth in Cd-and Ni-contaminated soils. Letters in Applied Microbiology 47, 561-565. [ Links ]
Karavangeli, M., Labrou, N.E., Clonis, Y.D. y Tsaftaris, A. (2005). Development of transgenic tobacco plants overexpressing glutathione S-transferase I for chloroacetanilide herbicides phytoremediation. Biomolecular Engineering 22, 121-128. [ Links ]
Kavamura, V.N. y Esposito, E. (2010). Biotechnological strategies applied to the decontamination of soils polluted with heavy metals. Biotechnology Advances 28, 61-69. [ Links ]
Kidd, P., Barcelo, J., Bernal, M.P., Navari-Izzo, F., Poschenrieder, C., Shileve, S., Clemente, R. y Monterroso, C. (2009). Trace element behaviour at the root-soil interface: Implications in phytoremediation. Environmental and Experimental Botany 67, 243-259. [ Links ]
Kuiper, I., Lagendijk, E.L., Bloemberg, G.V. y Lugtenberg, B.J.J. (2004). Rhizoremediation: a beneficial plant-microbe interaction. Biology of Plant-Microbe Interactions 17, 6-15. [ Links ]
Lee, S.H., Lee, W.S., Lee, C.H. y Kim, J.G. (2008). Degradation of phenanthrene and pyrene in rhizosphere of grasses and legumes. Journal of Hazardous Materials 153, 892-898. [ Links ]
Li, W.C., Ye, Z.H. y Wong, M.H. (2010). Metal mobilization and production of short-chain organic acids by rhizosphere bacteria associated with a Cd/Zn hyperaccumulating plant, Sedum alfredii. Plant and Soil 326,453-467. [ Links ]
Liu, H., Weisman, D., Ye, Y., Cui, B., Huang, Y., Colon-Carmona, A. y Wang, Z. (2009). An oxidative stress response to polycyclic aromatic hydrocarbon exposure is rapid and complex in Arabidopsis thaliana. Plant Science 176, 375-382. [ Links ]
Ma, L.Q., Komart, K.M., Tu, C., Zhang, W., Cai, Y. y Kennelley, E.D. (2001). A fern that hyperaccumulates arsenic. Nature, 409, 579. [ Links ]
Maldonado, A., Favela-Torres, E., Rivera-Cabrera, F. y Volke-Sepulveda, T. (2011). Lead bioaccumulation in Acacia farnesiana and its effect on lipid peroxidation and glutathione production. Plant and Soil 339, 377-389. [ Links ]
Marr, L., Booth, E., Andersen, R., Widdowson, M. y Novak, J. (2006). Direct volatilization of naphthalene to the atmosphere at a phytoremediation site. Environmental Science and Technology 40, 5560-5566. [ Links ]
Martí, M.C., Camejo, D., Fernandez-García, N., Rellán-Aí lvarez, R., Marques, S., Sevilla, F. y Jiménez, A. (2009). Effect of oil refinery sludges on the growth and antioxidant system of alfalfa plants. Journal of Hazardous Materials 172, 879-885. [ Links ]
Meagher, R.B. (2000). Phytoremediation of toxic elemental and organic pollutants. Current Opinion in Plant Biology 3, 153-162. [ Links ]
Mench, M., Schwitzguébel, J., Schroeder, P., Bert, V., Gawronski, S. y Gupta, S. (2009). Assessment of successful experiments and limitations of phytotechnologies: contaminant uptake, detoxification and sequestration, and consequences for food safety. Environmental Science and Pollution Research 16, 876-900. [ Links ]
Mertens, J., Vervaekea, P., De Schrijver, A., Luyssaert, S. 2004. Metal uptake by young trees from dredged brackish sediment: limitations and possibilities for phytoextraction and phytostabilisation. Science of the Total Environment 326, 209-215. [ Links ]
Meyer, A.J. (2008). The integration of glutathione homeostasis and redox signaling. Journal of Plant Physiology 165, 1390-1403. [ Links ]
Mills T., Arnold B., Sivakumaran S., Northcott G. , Vogeler I., Robinson B., Norling C. y Leonil D. (2006). Phytoremediation and long-term site management of soil contaminated with pentachlorophenol (PCP) and heavy metals. Journal of Environmental Management 79, 232-241. [ Links ]
Mittler, R. (2002). Oxidative stress, antioxidants y stress tolerance. Trends in Plant Science 7,405-410. [ Links ]
Møller, I.M. (2001). Plant mitochondria and oxidative stress: electron transport, NADPH turnover, and metabolism of reactive oxygen species. Annual Review of Plant Physiology and Plant Molecular Biology 52, 561-591. [ Links ]
Møller, I.M., Jensen, P.E. y Hansson, A. (2007). Oxidative modifications to cellular components in plants. Annual Review of Plant Biology 58, 459-481. [ Links ]
Moreno, F.N., Anderson, C.W.N., Stewart, R.B. y Robinson, B.H. (2005). Mercury volatilisation and phytoextraction from base-metal mine tailings. Environmental Pollution 136, 341-352. [ Links ]
Pilon-Smits, E. (2005). Phytoremediation. Annual Review of Plant Biology 56, 15-39. [ Links ]
Rezek, J., in der Wiesche, C., Mackova, M., Zadrazil, F. y Macek, T. (2008). The effect of ryegrass (Lolium perenne) on decrease of PAH content in long term contaminated soil. Chemosphere 70, 1603-1608. [ Links ]
Rinalducci, S., Murgiano, L. y Zolla, L. (2008). Redox proteomics: basic principles and future perspectives for the detection of protein oxidation in plants. Journal of Experimental Botany 59, 3781-3801. [ Links ]
Rotkittikhun, P., Chaiyarat, R., Kruatrachue, M., Pokethitiyook, P. y Baker, A.J.M. (2007). Growth and lead accumulation by the grasses Vetiveria zizanioides and Thysanolaena maxima in lead-contaminated soil amended with pig manure and fertilizer: A glasshouse study. Chemosphere 66, 45-53. [ Links ]
Sharma, S.S. y Dietz, K.J. (2008). The relationship between metal toxicity and cellular redox imbalance. Trends in Plant Science 14, 43-50. [ Links ]
Singh, O.V., Labana, S., Pandey, G., Budhiraja, R. y Jain, R.K. (2003). Phytoremediation: an overview of metallic ion decontamination from soil. Applied Microbiology and Biotechnology 61, 405-412. [ Links ]
Singh, N., Ma, L.Q., Srivastava, M. y Rathinasabapathi, B. (2006). Metabolic adaptations to arsenic-induced oxidative stress in Pteris vittata L and Pteris ensiformis L. Plant Science 170, 274-282. [ Links ]
Soleimani, M., Afyuni, M., Hajabbasi, M.A., Nourbakhsh, F., Sabzalian, M.R. y Christensen, J.H. (2010). Phytoremediation of an aged petroleum contaminated soil using endophyte infected and non-infected grasses. Chemosphere 81, 1084-1090. [ Links ]
Sun, Q., Ye, Z.H., Wang, X.R. y Wong, M.H. (2005). Increase of glutathione in mine population of Sedum alfredii: a Zn hyperaccumulator and Pb accumulator. Phytochemistry 66, 2549-2556. [ Links ]
Tausz, M., Sircelj, H. y Grill, D. (2004). The glutathione system as a stress marker in plant ecophysiology: is a stress-response concept valid? Journal of Experimental Botany 55, 1955-1962. [ Links ]
Triantaphylides C. y Havaux M. (2009). Singlet oxygen in plants: production, detoxification and signaling. Trends in Plant Science 14, 219-228. [ Links ]
Unterbrunner, R., Puschenreiter, M., Sommer, P., Wieshammer, G., Tlustos, P., Zupan, M. y Wenzel W.W. (2007). Heavy metal accumulation in trees growing on contaminated sites in Central Europe. Environmental Pollution 148, 107-114. [ Links ]
Vangronsveld, J., Herzig, R., Weyens, N., Boulet, J., Adriaensen, K., Ruttens, A., Thewys, T., Vassilev, A., Meers, E., Nehnevajova, E., van der Lelie, D. y Mench, M. (2009). Phytoremediation of contaminated soils and groundwater: lessons from the field. Environmental Science and Pollution Research 16, 765-794. [ Links ]
Wenzel, W.W., Bunkowskia, M., Puschenreitera, M. y Horak, O. (2003). Rhizosphere characteristics of indigenously growing nickel hyperaccumulator and excluder plants on serpentine soil. Environmental Pollution 123, 131-138. [ Links ]
1 Las plantas hiperacumuladoras incluyen especies que acumulan en sus tejidos aéreos (%, peso seco): > 1 de Mn o Zn, > 0.1 de Cu, Co, Cr, Ni o Pb, > 0.01 de Cd (Wenzel y col., 2003).
2 Este tipo de plantas sobrevive y acumula mínimas cantidades de metales es en sus tejidos, aún en lugares muy contaminados (Wenzel y col., 2003; Wei y col., 2005).
3 Proceso por el cual un organismo mantiene constantes las condiciones celulares necesarias para la vida.
4 Un radical libre se refiere a una especie que contiene uno o más electrones no apareados (Halliwell, 2006).
5 Reacción Haber-Weiss completa: ·O-2 + H2O2 → -OH + ·OH + O2 Esta reacción es catalizada por Fe3+ mediante una reacción Fenton y es el principal mecanismo de producciónde ·OH en sistemas biologicos (Halliwell, 2006): ·O-2 + Fe3+ → O2 + Fe2+ H2O2 + Fe2+ → -OH + ·OH + Fe3+ (reacción Fenton)
6 El término anitoxidante describe cualquier compuesto capaz de disminuir los niveles de ERO sin que, por sí misma, se convierta en un radical destructivo (Gratão y col., 2005).
Fuente:http://www.scielo.org.mx/scielo.php?pid=S1665-27382012000100006&script=sci_arttext
No hay comentarios:
Publicar un comentario